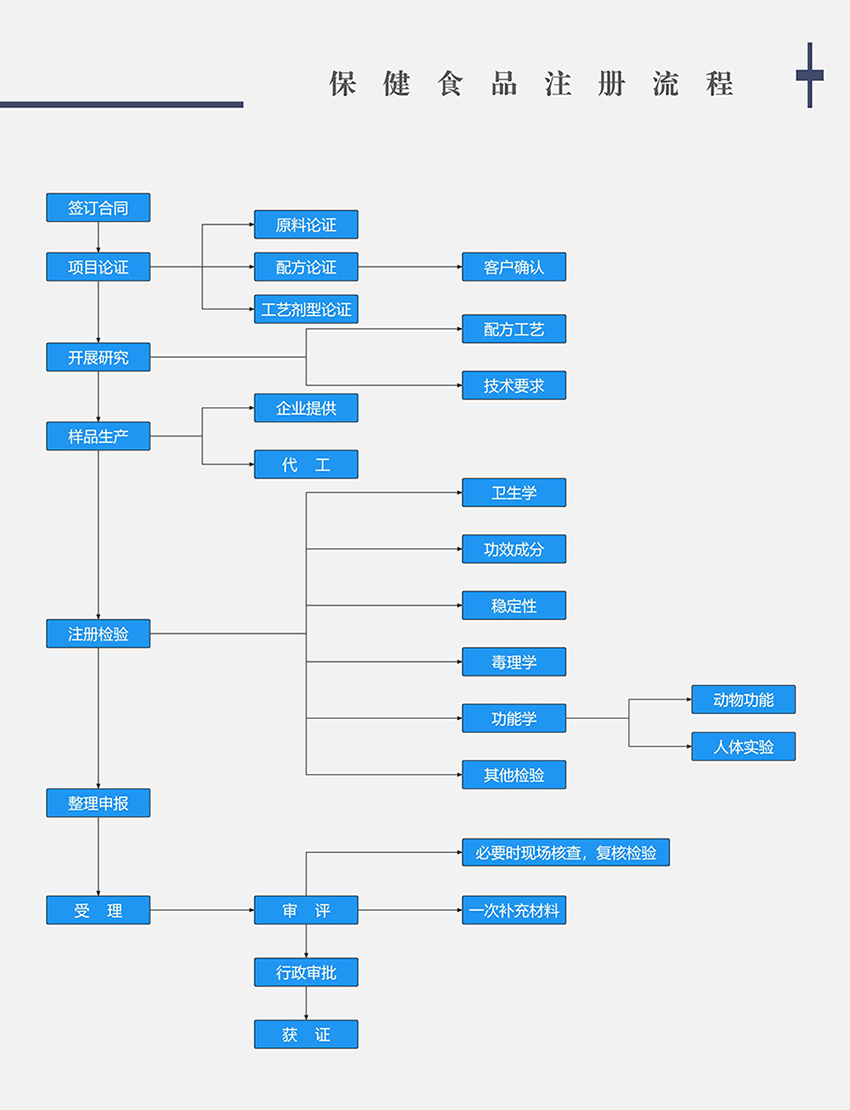
一、保健食品注册流程
1.准备申请材料:
包括保健食品注册申请表,申请人对申请材料真实性负责的法律责任承诺书,注册申请人主体登记证明文件复印件等十项材料(具体可参考《保健食品注册与备案管理办法》第十二条)。如果是申请初次进口保健食品注册,还需提交产品生产国相关的资质证明文件、上市销售证明文件等材料(具体可参考《保健食品注册与备案管理办法》第十三条)。
2.提交申请:
将准备好的申请材料提交至国家食品药品监督管理总局行政受理机构。
3.受理:
受理机构收到申请材料后,根据不同情况分别作出处理,如申请事项依法不需要取得注册的,即时告知申请人不受理;申请材料不齐全或者不符合法定形式的,当场或者在5个工作日内一次告知申请人需要补正的全部内容等。符合受理条件的,予以受理并出具加盖专用章和注明日期的书面凭证。
4.审评:
受理后,申请材料送交审评机构。审评机构组织审评专家对申请材料进行审查,并根据实际需要组织开展现场核查、复核检验,在60个工作日内完成审评工作,向国家食品药品监管管理总局提交综合审评结论和建议。特殊情况下可延长20个工作日。
5.注册决定:
国家食品药品监督管理总局自受理之日起20个工作日内对审评程序和结论进行审查,作出准予注册或者不予注册的决定。
证书发放或不予注册通知:
国家食品药品监督管理总局作出决定后,自作出决定之日起10个工作日内,由受理机构向注册申请人发出保健食品注册证书或者不予注册决定。
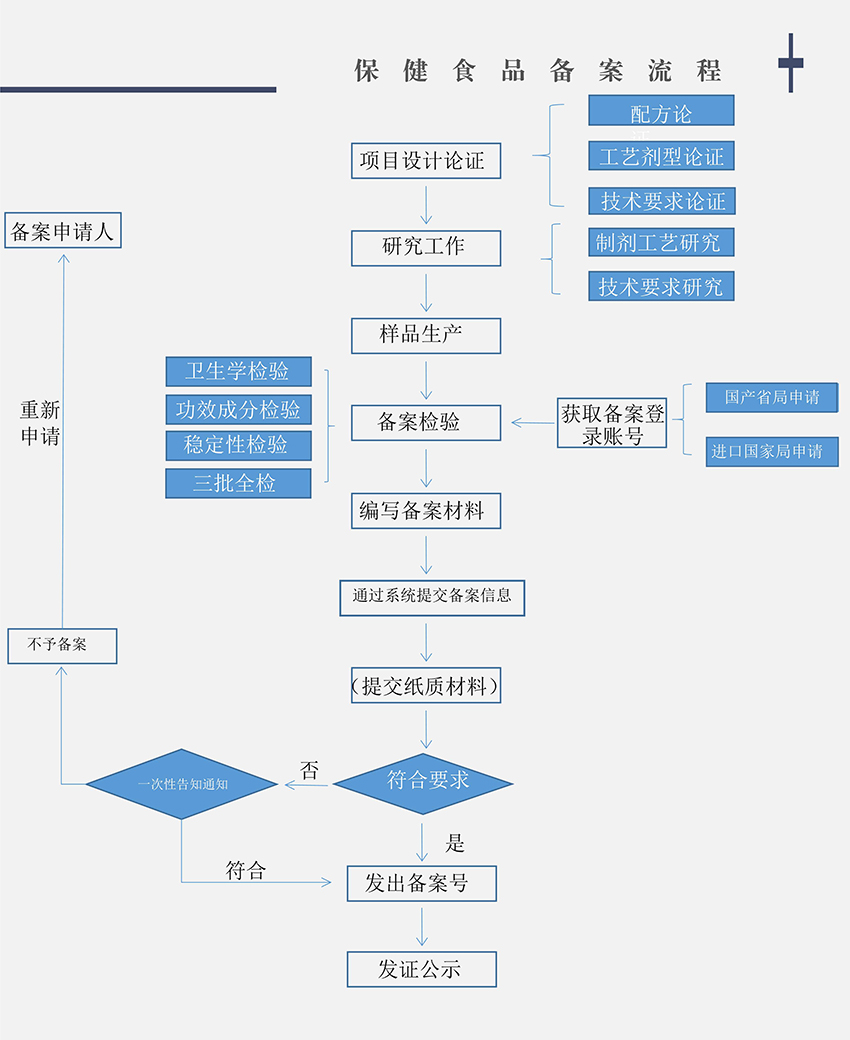
二、保健食品备案流程
1. 获取备案系统登录账号:
国产保健食品备案人向所在地省、自治区、直辖市食品药品监督管理部门提出申请;进口保健食品备案人携带相关资质证明文件和联系人授权委托书等,向国家食品药品监督管理总局行政受理服务部门现场提出申请;原注册人产品转备案的,向总局技术审评机构提出申请。
2. 产品备案信息填报、提交:
备案人获得登录账号后,通过指定网址进入系统,填写备案人及申请备案产品相关信息,打印系统自动生成的相关材料,加盖公章后,将所有备案纸质材料扫描成彩色电子版(PDF格式)上传至系统,确认后提交。进口保健食品备案人还需向国家食品药品监督管理总局行政受理服务部门提交全套备案材料原件1份。
3. 发放备案号、存档和公开:
备案材料符合要求的,备案管理部门当场备案,发放备案号,并制作备案凭证;不符合要求的,一次告知备案人补正相关材料。备案人应保留一份完整的备案材料存档备查。